4.DESINFECÇÃO e 5.ESTERILIZAÇÃO
 |
| Fonte: http://www.prolab.com.br/ |
(Microbiologia Básica / Profa . Zilka Nanes Lima)
Página atualizada em 10/11/2025
Creative Commons(by-nc-nd) ZILKA NANES LIMA(2025).
Atribuição-NãoComercial-SemDerivações.
ASSUNTOS: DESINFECÇÃO
DE SUPERFÍCIES /
ISOLAMENTO DE MICRO-ORGANISMOS DE SUPERFÍCIES INANIMADAS/ ESTERILIZAÇÃO EM LABORATÓRIO DE MICROBIOLOGIA/ PREPARAÇÃO E DISTRIBUIÇÃO DE MEIOS DE CULTURA
ISOLAMENTO DE MICRO-ORGANISMOS DE SUPERFÍCIES INANIMADAS/ ESTERILIZAÇÃO EM LABORATÓRIO DE MICROBIOLOGIA/ PREPARAÇÃO E DISTRIBUIÇÃO DE MEIOS DE CULTURA
Glossário
Assepsia (HIGIENIZAÇÃO PREVENTIVA DO AMBIENTE)
1) Consiste num conjunto de métodos e processos de higienização de determinado ambiente, com a finalidade de evitar a contaminação do mesmo por agentes infecciosos e patológicos.
1) Feita através do uso de substâncias químicas, como microbicidas, por exemplo, que visam eliminar ou diminuir a proliferação das bactérias (ou demais micro-organismos indesejados), seja num organismo vivo ou num ambiente.
2) É
o método através do qual se impede a proliferação de micro-organismos em
tecidos vivos com o uso de substância químicas (os anti-sépticos).
3)
A
mesma substância química usada em objetos inanimados será chamada de
desinfetante. E quando usada em tecidos vivos será chamada de anti-séptico. Ex. clorexidina e iodopovidina.
Autoclave
1)
É um aparelho utilizado para esterilizar vidrarias, meios de cultura, algodão, gaze etc., através
do calor úmido sob pressão. Inventado por Charles Chamberland, auxiliar de
Louis Pasteur.
2)
Nada mais é do que uma câmara com força
suficiente para suportar pressões de 20 até 30 libras por cm2 e,
eventualmente, suportar também alto vácuo
Esterilização
1)
Tornar
estéril ou livre de micro-organismos. Tornar incapaz de se reproduzir
2)
Inativação
total de todos os micro-organismos quanto à capacidade reprodutiva
3)
Esterilização
acontece por calor seco, calor úmido, raios gama, raios X e compostos químicos.
.
Desinfecção
1)
Destruição
dos micro-organismos por meios químicos ou físicos aplicados diretamente em
superfícies inanimadas.
2)
Processo
que reduz o número de bactérias contaminantes a um “nível razoável de
segurança” mas que não se aplica necessariamente, na eliminação de todos os
microrganismos viáveis.
1.a) DESINFECÇÃO DE
SUPERFÍCIES:
Na
desinfecção de superfícies podem ser utilizados: álcool a 70% (ou 77o
GL); compostos sintéticos de iodo; compostos fenólicos; hipoclorito de sódio ou
solução alcoólica de clorexidina. Atualmente, tem sido preconizada a técnica spray-wipe-spray, cuja técnica inclui a
pré-limpeza e a desinfecção, e consiste em aplicar o desinfetante na superfície
com auxílio de um borrifador; a seguir, limpar a área com toalha de papel e
realizar nova aplicação do desinfetante.
Tabela 1. Atividade antimicrobiana das principais
classes de desinfetantes, anti-sépticos e esterilizantes
Agente
|
Bactérias Gram +
|
Bactérias Gram -
|
Esporos bacterianos
|
Fungos
|
M.tuberculosis*
|
HIV**
|
HBV***
|
Halogênios (1)
|
+
|
+
|
±
|
+
|
±
|
+
|
+
|
Aldeídos (2)
|
+
|
+
|
+
|
+
|
+
|
+
|
+
|
Fenóis (3)
|
+
|
+
|
(-)
|
+
|
+
|
+
|
+
|
Compostos de amônio quaternário (4)
|
+
|
+
|
(-)
|
±
|
(-)
|
(-)
|
(-)
|
Álcóois (5)
|
+
|
+
|
(-)
|
±
|
+
|
+
|
+
|
Clorexidina
|
+
|
+
|
(-)
|
±
|
(-)
|
+
|
(-)
|
Gram + = Gram-positivas; Gram - = Gram-negativas; * Mycobacterium
tuberculosis; (O M.
tuberculosis é mais
resistente aos desinfetantes químicos que qualquer outra bactéria não
esporulante). ** HIV: vírus da imunodeficiência humana; *** HBV:vírus da hepatite B.
+ = tem atividade antimicrobiana; ± =moderada atividade antimicrobiana (-)
= não tem atividade antimicrobiana. (1) Flúor, cloro, iodo; (2) Formaldeído e
glutaraldeído; (3) Hexaclorofeno, policresuleno, cloroxilenol; (4) Cloreto de
benzalcônio, cetrimida. (5) Etanol e isopropanol.
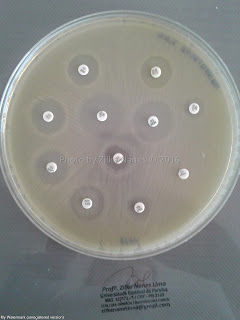
Os agentes
químicos podem ser classificados de acordo com a eficácia em 3 grupos
principais:
- Alto
nível: Promovem a esterilização
dos materiais. Agem contra fungos, bactérias Gram-positivas e Gram-negativas,
esporos bacterianos e vírus.
- Nível
intermediário: Capazes de
destruir quase todas as formas de microrganismos, a exceção dos esporos.
- Baixo
nível: Não agem contra
o vírus da hepatite, poliomielite, esporos e Mycobacterium tuberculosis.
1.b)
TÉCNICA PARA ISOLAMENTO DE MICRO-ORGANISMOS DE SUPERFÍCIES INANIMADAS (ANTES E
APÓS O USO DE ÁLCOOL A 70%)
A) Material necessário:
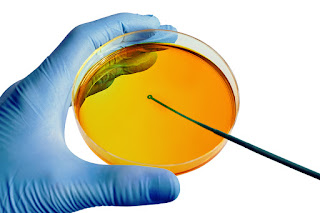
- Placa de Petri com Agar Sangue (ou outro Meio de
cultura não seletivo)
- Lápis marcador
- Dois swabs esterilizados
- Tubo com 2 mL de solução fisiológica
- Frasco contendo álcool a 70%
- Papel toalha
B) Procedimento
- Dividir o fundo da placa de Petri contendo o ágar
Sangue em duas partes com lápis para vidro, e identificar a placa;
- Pegar um swab estéril, umedecê-lo em salina estéril
e esfregar sobre a bancada . A seguir semear metade da placa com o swab
identificando “antes”;
- Realizar desinfecção da bancada com álcool a 70%,
esperar 2 minutos. A seguir utilizando-se de outro swab estéril umedecido em
salina também esterilizada, esfregar na bancada e semear na segunda parte do
meio de cultura. Identificar: “depois”.
- Incubar as placas em estufa bacteriológica à 36oC
por 24 horas. Observar e discutir o resultado.
2. PREPARAÇÃO E DISTRIBUIÇÃO DE MEIOS DE CULTURA
MEIOS
DE CULTURA: Antes de descrever a técnica de preparação de
meios de cultura o bacteriologista precisa saber os tipos de meios de cultura; como
esterilizar estes meios, as placas de Petri, a vidraria e todo o material
utilizado no Laboratório de Microbiologia Básica. A esterilização do meio de cultura é realizada após a sua hidratação,
visando eliminar os micro-organismos contaminantes.
Meios
de cultura - Quanto à consistência:
- Sólidos: tem 1,5% de ágar. Nele
obtemos crescimento de colônias isoladas.
- Semi-sólidos: adição de menor
quantidade de ágar, utilizado para leitura de motilidade bacteriana.
- Líquidos ou caldos: Não contêm ágar, utilizado
para obter enriquecimento de micro-organismos por turvação do meio.
Meios de cultura -
Quanto à função e conteúdo químico:
De acordo com seu conteúdo químico, os meios de
cultura podem ser sintéticos ou complexos.
1.
Meio de Enriquecimento: Geralmente líquido, de
composição química rica em nutrientes, com a finalidade de permitir que as
bactérias contidas em uma amostra clínica aumentem em número.
Ex.: Caldo Brain Heart
Infusion (BHI) e CaldoTetrationato.
2.
Meio não seletivo: Tem na sua composição
nutrientes básicos para todos os micro-organismos não-fastidiosos e de fácil
crescimento. Ex: Agar sangue, Agar BAB (Blood Ágar Base), ágar CLED (Cystine
Lactose Eletrolyte Deficient).
3.
Meio Seletivo: A finalidade deste tipo
de meio é selecionar as espécies que se deseja isolar e impedir o
desenvolvimento de outros germes (têm na sua composição adição de corantes,
antibióticos e outras substâncias com capacidade inibitória para
micro-organismos determinados). Ex.: Agar Manitol Salgado, Agar SS, Agar
MacConkey e Agar Eosin Methilene Blue (EMB).
4.
Meio Diferencial: Possibilita a distinção
entre vários gêneros e espécies de microrganismos, por possuir substâncias que
permitem uma diferenciação presuntiva, evidenciada na mudança de coloração ou
na morfologia das colônias.
Ex.: Agar Eosin Methilene Blue (EMB), Agar MacConkey e Agar Hektoen.
5.
Meio Indicador: É utilizado no estudo das propriedades
bioquímicas das bactérias, auxiliando, assim sua identificação. O mais simples
é aquele usado no estudo das reações de fermentação. Ex.: Agar Triple Sugar
Iron (TSI), Agar Citrato de Simmons, Agar Eosin Methilene Blue
(EMB), Agar MacConkey e Agar Hektoen.
Meio
de Transporte (não é um ‘meio de cultura’):
Consiste em um meio isento de nutrientes, contendo um agente redutor (cisteína).
Geralmente mantém o pH favorável, previne a desidratação de secreções durante o
transporte e evita a oxidação e auto-destruição enzimática dos patógenos
presentes.
Ex.: Meio de Stuart e Meio de Cary-Blair.
ESTERILIZAÇÃO
EM LABORATÓRIO DE MICROBIOLOGIA
CALOR ÚMIDO SOB PRESSÃO (AUTOCLAVAÇÃO)
Durante a autoclavação ocorre na estrutura orgânica dos
microrganismos desnaturação protéica, coagulação de proteínas e de enzimas,
fusão de lipídeos da membrana celular.
Para obtermos vapor saturado devemos expulsar todo ar
livre, da autoclave. A presença desse ar faz variar a temperatura obtida no
processo, impedindo, ás vezes, que haja uma esterilização eficiente.
Um
fator de grande importância na exaustão completa do ar da autoclave é que
geralmente as temperaturas de autoclavação são medidas por manômetros de
pressão, em função das relações conhecidas e não diretamente por termômetros.
É importante que a água seja sempre trocada (usar água
destilada) para esterilização de meios de cultura, para evitar uma contaminação
química dos mesmos. Convém utilizar uma autoclave especialmente, para a
produção de meios de cultura e outro para esterilizar todo o material
contaminado.
Como
utilizar a autoclave:
1)
Repor
a água no nível indicado (geralmente logo abaixo da grade de suporte de
material, a grade vista por cima tem forma de X);
2)
Carregar
a autoclave, colocando a vidraria maior embaixo e pequenos tubos dentro de
cestas na parte superior, deixando espaço entre os materiais para permitir que
o vapor circule entre os componentes e evite quebra da vidraria;
3)
Fechar
a tampa, verificar se a borracha está encaixada, apertar os fechos de segurança
simetricamente e deixar a válvula de escape aberta;
4)
Ligar
as duas resistências (geralmente ligadas a 220V). Ligar a chave geral e depois
a chave da autoclave no máximo (ATENÇÂO: Aumentar a chave da autoclave passando
de DESLIGADO para MÍNIMO, depois MÉDIO até chegar em MÁXIMO). Deixar no MÁXIMO
e esperar a emanação de vapor fluente, ininterrupto, pela válvula de escape;
5)
Vapor
fluente emanando, fechar a válvula de escape e esperar até que o manômetro
atinja a pressão desejada (1 atm ou 121oC). Passar então para o
MÉDIO (algumas autoclaves no MÍNIMO);
6)
Marcar
o tempo de esterilização (15 minutos para meios de cultura e 30 minutos para
material contaminado). Se a pressão desejada cair, colocar no MÁXIMO até chegar
novamente em 1 atm; se a pressão desejada aumentar colocar no mínimo ou
desligar as resistências;
7)
Terminado
o tempo de autoclavação desligar as resistências e esperar a pressão voltar a
zero. Abrir a válvula de escape, esperar o vapor sair. Abrir a autoclave e
retirar o material.
PS: Melhor vídeo que encontrei no Youtube sobre o uso da autoclave.
Para ser perfeito a moça deveria está usando EPIs.
Figura 1 - Autoclave vertical de 30 litros do Laboratório de análises clínicas da UEPB
 |
| Fonte; Autora (arquivo pessoal) |
CALOR
SECO (ESTUFA DE ESTERILIZAÇÃO)
Na
estufa esterilizamos toda a vidraria (Placas de Petri, pipetas de vidro, tubos
de vidro com tampas de algodão etc.). Para facilitar o trabalho na hora da
distribuição dos meios de cultura, faça os pacotes com placas de mesmo tamanho
e as deixe na mesma posição (todas com a tampa para cima ou para baixo).
ATENÇÃO: Quando usar algodão é preferível utilizar o calor úmido, caso utilize
o calor seco proteja o algodão com papel.
O
material deve ser embrulhando com papel manteiga ou papel kraft. Fazendo
pacotes semelhantes aos de mercearia, com extremidades bem presas.
A
estufa deve ser preenchida de maneira que o papel não toque nas paredes.
Ajustar
o termostato da estufa. Ligar, esperar a temperatura atingir 175º C, e então
marcar 2 horas. Após este tempo, desligar e esperar esfriar para então retirar
o material.
PS:
Caso a estufa ultrapasse a temperatura desejada, desligue o botão ON-OFF e
depois retire da tomada. Não abra antes de esfriar.
PARA
DISTRIBUIÇÃO DOS MEIOS DE CULTURA - NUNCA
ESQUECER:
®
Antes de utilizar a sala de meios de cultura, fechar a porta da sala, ligar a
luz ultravioleta por 30 minutos. O interruptor fica do lado de fora da sala,
ele ligará a luz UV (que fica dentro da sala) e a luz de alerta – vermelha (que
fica fora da sala na parte superior da porta);
® Deve ter-se sempre presente que a
lâmpada UV só deve estar ligada na ausência de pessoas no interior da sala.
® Certificar-se de que ao dar início às operações, todo o material
necessário está ao alcance imediato, de forma a realizar o trabalho o mais
rapidamente possível
®
Certificar-se que não exista nenhuma corrente de ar, que possa a vir contaminar
os meios de cultura.
® Desinfetar (com álcool à 70%) e arrumar convenientemente a
bancada de trabalho
® Utilizar
luvas, máscaras e óculos de proteção individual. Evitar falar durante a
distribuição dos meios de culturas.
® Os recipientes devem estar abertos o mínimo tempo possível e,
enquanto abertos, todo o trabalho deve ser realizado preferencialmente junto à
chama do bico de Bunsen
® Uma vez abertos os recipientes, como tubos, balões e frascos, o
seu bocal deve ser flamejado de imediato
® A fim de evitar as contaminações durante as manipulações que
envolvam placas de Petri, a exposição das superfícies internas estéreis deve
durar o mínimo de tempo possível
®
Deixar os meios de cultura, após autoclavados atingirem a temperatura ideal
(45-55ºC) para distribuir, pois se muito quente forma-se água de condensação
que facilita a contaminação.
®
Sempre guardar as placas após prontas com a tampa para baixo e o meio para cima
- em geladeira, dentro das jarras de microaerofilia, em estufa - a única
exceção é na hora da esterilização de placas contaminadas – que coloca-se em
autoclave com a tampa para cima dentro de sacos plásticos que suportem o calor
úmido (121ºC por 30 minutos).
® Não
distribuir os meios em qualquer material e tamanho de placa.. O tamanho vai
depender da finalidade e de que métodos estamos utilizando, o material da placa
também (vidro ou plástico).
Referências bibliográficas:
- Jorge, A.O.C.. Microbiologia: atividades práticas 2a
edição. Ed. Santos. São Paulo, SP, 2008
- Oplustil, C.P.; Zoccoli, C.M.;
Tobouti, N.R.; Sinto, S.I. Procedimentos
Básicos em Microbiologia Clínica 3a
edição.Ed.
Sarvier, São Paulo- SP, 2010.

Comentários
Postar um comentário
Olá! Comente abaixo sua opinião a respeito do nosso blog, ajudará a manter nosso projeto ativo. Obrigada!